Stage de spectrographie - Session 2 (1/4)
LA CONSTRUCTION D'UN SPECTROGRAPHE
Aude - Bonjour Christian, Raymond, Alain. Vous avez vu lors de la session prťcťdente de ce stage qu'il est possible de rťaliser de l'analyse spectrale d'objets astronomiquement sans trop d'effort. Dans cette session nous allons apprendre ŗ concevoir et utiliser un spectrographe un peu plus ťvoluť, qui va offrir comme il se doit de nouvelle possibilitť.
Raymond - Chic, Áa me plaÓt. Avec un tel engin j'ai pouvoir d'observer le Soleil, les ťtoiles, les nťbuleuses, les galaxies...
Aude - Je t'arrÍte Raymond. Tu me parais trŤs enthousiaste et je ne veux pas briser cela. Mais sache que le grand dilemme de la spectrographie est le compromis entre la rťsolution spectrale et la capacitť d'observer des objets faibles. On a entrevu cette problťmatique lors de la premiŤre session.
Christian - Avant de faire de la technique, j'aimerais que tu nous en dises plus sur la signification physique des couleurs que l'on voit dans un spectre.
Aude - D'accord, c'est important - je vais faire quelques rappels et entrer un peu plus dans les dťtails. La couleur trahit une caractťristique fondamentale de la lumiŤre. La perception visuelle des couleurs par est liťe ŗ la maniŤre dont l'oeil traduit cette caractťristique physique. Au lieu de parler de nuances colorťs, une notion assez subjective, on a dťjŗ vu que les physiciens prťfŤrent parler de longueur d'onde. Ils reprťsentent souvent la lumiŤre comme une onde sinusoÔdale qui se propage dans l'espace ŗ la vitesse de 299792,458 km/s. C'est la distance parcourue sur une pťriode de cette sinusoÔde que l'on appelle longueur d'onde. Cette quantitť est gťnťralement dťsignťe par la lettre grecque l (lambda). Voici par exemple deux ondes lumineuses avec des longueurs distinctes l1 et l2 :
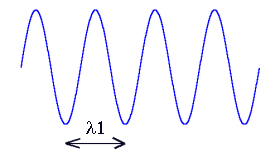
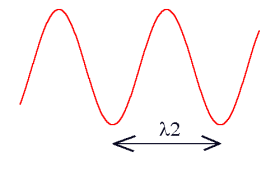
Les courtes longueurs d'ondes sont associťes ŗ la couleur bleue dans le spectre visible, alors que les grandes longueurs d'ondes produisent la sensation de rouge. Ce qui est vraiment important ŗ comprendre c'est qu'ŗ chaque couleur perÁue par l'oeil est associťe une longueur d'onde. Voici les valeurs usuelles de cette longueur pour le spectre visible en nanomŤtre (1 nanomŤtre = 1.10-6 mm).

Par exemple, un rayon lumineux de longueur d'onde de 450 nm sera vu par l'oeil d'un bleu extrÍmement profond. Cette longueur est petite : 0,45 micron, ou si on prťfŤre un 450 milliardiŤmes de mŤtre ! Un capteur CCD courant peu dťtecter quant ŗ lui la lumiŤre jusqu'ŗ une longueur d'onde de 1000 nm, ce qui double pratiquement le domaine spectral observable par rapport ŗ ce que voie l'oeil.
Alain - Tu nous a dit que la longueur d'onde pouvait s'exprimer dans une unitť bizarre, en angstrŲms. C'est bien Áa ?
Aude - Oui, tout ŗ fait. L'angstrŲm est une unitť de longueur fort usitťe par les spectromťtriste. On la note par la lettre Ň. Il y a une relation simple entre l'angstrŲm et le nanomŤtre : 1 Ň= 0,1 nm. Le milieu du spectre visible correspond ainsi ŗ une longueur d'onde de 5700 angstrŲms environ.
Christian - Tous les objets lumineux ont un spectre alors ?
Aude - Oui, mais l'allure de ce spectre peut Ítre trŤs diffťrente d'un objet ŗ l'autre. Avec la plupart des ťtoiles, un examen rapide du spectre montre que celui-ci passe rťguliŤrement du bleu au rouge, sans interruption des couleurs. On dit que le spectre est continu. En y regardant de plus prŤs, on constate que gťnťralement le spectre comprend des zones ťtroites oý la lumiŤre est pratiquement absente. On appelle ces zones des raies d'absorption. Elles sont la signature spectrale des ťlťments chimiques prťsents dans l'atmosphŤre de l'ťtoile. Dans certaines conditions physiques, les raies apparaissent en ťmission, c'est ŗ dire plus lumineuses que le continuum qui les entoure. Le spectre simulť ci-aprŤs montre ŗ la fois des raies en absorption et une raie en ťmission dans le rouge, cette derniŤre, ŗ la longueur d'onde de 6563 angstrŲms, ťtant probablement provoquťe par les atomes d'hydrogŤne.

L'enregistrement des spectres permet d'identifier ŗ distance les ťlťments constituant l'objet observť et les conditions physiques qui rŤgne dans le milieu oý est produite cette lumiŤre. Cela montre l'intťrÍt considťrable de la spectrographie, notamment en astronomie...
Christian - Je t'arrÍte Aude. Qu'est-ce qui te permet de dire qu'une raie est associťe ŗ l'hydrogŤne dans ton exemple ?
Aude - J'ai ťtť un peu vite. Pour comprendre il faut pťnťtrer dans la structure intime de l'atome. Prenons l'exemple de l'atome d'hydrogŤne, le plus simple. Il est constituť d'un noyau autour duquel gravite un ťlectron sur une orbite circulaire ŗ une certaine distance du noyau. C'est une vision simpliste et trŤs imagťe de ce qu'est un atome, mais correcte pour expliquer bon nombre des phťnomŤnes observťs en spectrographie. L'ťlectron peu changer d'orbite sous certaines conditions, mais les rayons de ces orbites ne peuvent Ítre quelconques. Les rayons des orbites sont codifiťs, on dit en physique, quantifiťs. Un ťlectron ne pourra ainsi circuler de maniŤre stable que sur quelques orbites prťdťfinies. Les atomes de tous les ťlťments chimiques suivent des orbites du mÍme type, mais en fonction de l'ťlťment chimique, les rayons de ces orbites stables ne seront pas les mÍmes. Cette diffťrence est fondamentale, car c'est elle qui permet de distinguer tel ou tel ťlťments chimiques dans un spectre en analysant la position des raies.
Christian - D'accord, mais je ne vois toujours pas ce qui produit ces raies !
Aude -
J'y viens. Pour qu'un ťlectron passe d'une orbite stable infťrieure
ŗ une orbite stable supťrieure, c'est ŗ dire vers un plus
grand rayon, il est nťcessaire de lui transmettre de l'ťnergie.
C'est la mÍme ťnergie que vous devez dťpenser lorsque vous
montez un barreau d'une ťchelle. Or, il se trouve que la lumiŤre
porte en elle cette ťnergie nťcessaire, qui est, c'est important,
d'autant plus grande que la longueur d'onde est courte. A prťsent, lorsqu'un
rayon lumineux passe ŗ proximitť d'un atome il peut transfťrer
une partie bien prťcise de son ťnergie ŗ l'ťlectron,
juste nťcessaire pour l'amener d'une orbite infťrieure ŗ
une orbite supťrieure donnťe. Cette ťnergie est transformťe
en quelque sorte en effort mťcanique pour faire grimper l'ťlectron
et elle disparaÓt alors du faisceau lumineux, car absorbťe par
l'atome. La couleur correspondante dans le spectre apparaÓtra noire. C'est
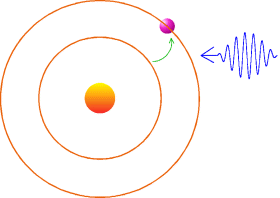
cela une raie spectrale. Voici une illustration de ce qui se passe. Le noyau
est en orange et l'ťlectron en violet. Suite ŗ un apport d'ťnergie,
sous la forme d'une onde lumineuse, l'ťlectron monte sur une des orbites
permises.
Christian - Cette couleur est toujours la mÍme alors ?
Aude - Oui, pour un ťlťment chimique donnť et un changement d'ťtage donnť. Mais dans un mÍme atome, un ťlectron peut trŤs bien sauter directement de l'ťtage 1 ŗ l'ťtage 3 par exemple. Pour cela il faudra qu'il absorbe une ťnergie supťrieure, de la mÍme maniŤre qu'il faudra dťpenser plus d'ťnergie pour monter deux barreaux sur une ťchelle plutŰt qu'un seul. Une nouvelle raie va apparaÓtre dans le spectre, correspondant ŗ l'ťnergie nťcessaire pour rťaliser ce changement d'orbite. De trŤs nombreuses combinaisons sont possibles. Par exemple, un ťlectron peut passer de l'orbite 3 a l'orbite 4 ou directement de l'orbite 2 ŗ l'orbite 4, et ainsi de suite. A chacune de ces combinaisons est associťe une raie spectrale spťcifique dans le spectre.
Raymond - Toutes ces raies sont donc visibles simultanťment dans le spectre !?
Aude - Non, c'est plus compliquť. Tout d'abord il faut que l'ťnergie qui permet de faire sauter un ťlectron d'un ťtage infťrieur ŗ un ťtage trŤs supťrieur soit disponible, ce n'est pas toujours le cas. Sous certaines conditions de pression et de tempťratures certains changement de niveau, on parle aussi de transitions atomiques, sont plus probables que d'autres. La non-prťsence des raies d'un ťlťment chimique dans le spectre ne signifie pas nťcessairement que cet ťlťment est absent du corps ťtudiť, simplement, les conditions physiques ne sont pas favorables pour que sa "signature" spectrale soit visible. Ceci explique pourquoi le spectre des ťtoiles froides et des ťtoiles chaudes est si diffťrent, alors que la composition chimique de l'ensemble des ťtoiles est relativement proche.
Christian - Et l'origine des raies en ťmission alors ?
Aude - C'est le processus inverse. Lorsque l'ťlectron passe d'une orbite supťrieure ŗ une orbite infťrieure il ťmet une sorte de bouffťe d'ťnergie qui prend la forme d'une onde de lumiŤre, que l'on appelle aussi quanta de lumiŤre ou photon. L'ťnergie transportťe dans l'onde correspond ŗ une raie ayant une position prťcise dans le spectre, prťdite dans le cadre d'une discipline de la physique que l'on nomme mťcanique quantique. Dans l'illustration je vous montre la crťation d'une onde lumineuse suite au passage d'un ťlectron d'une orbite supťrieure ŗ une orbite infťrieure :
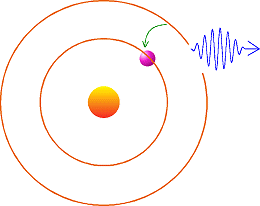
Cette onde porte une ťnergie bien prťcise prťdite par la mťcanique quantique pour la transition de l'ťlectron en question. Vous pouvez voir aussi la lumiŤre comme un grain d'ťnergie se dťplaÁant ŗ environ 300 000 km/s. Ce grain c'est la particule que l'on nomme photon. Pour faire la liaison avec le spectre vous pouvez attribuer une couleur ŗ un photon : un photon bleu sera plus ťnergťtique qu'un photon rouge.
Christian - Avec les raies en ťmission, suivant l'orbite de dťpart et l'orbite d'arrivťe, la longueur d'onde de la lumiŤre sera diffťrente, tout comme pour l'absorption ?
Aude - Exactement. Mais chaque atome d'un ťlťment chimique produit son propre spectre d'onde, une vťritable empreinte, qui est tout ŗ fait distincte de celles des autres ťlťments.
Alain - Tu as des exemples ?
Aude - Oui. Regardez ces spectres. Le premier est un spectre continu, sans aucunes raies. Puis de haut en bas vous avez le spectre d'ťmission de l'hydrogŤne, de l'hťlium, du sodium et de l'argon. Aucun ne se ressemble.





Christian - En effet !
Alain - Le spectre de l'argon contient un nombre incroyable de raies ! Ca a l'air simple finalement d'identifier un ťlťment chimique dans un spectre. Il suffit d'avoir son modŤle de raies.
Raymond - Il existe donc des catalogues de raies spectrales ?
Aude - C'est vrai que la signature spectrale des ťlťments chimiques se diffťrencie bien. On trouve dans des tables ou dans certains logiciels des catalogues de toutes les raies par ťlťment chimique. Mais vous devez imaginer la complexitť du problŤme d'identification si l'objet ťtudiť contient potentiellement tous les ťlťments chimiques. Les spectres individuels sont alors susceptibles de ce mťlangťs en un seul. Pas facile de reconnaÓtre les raies dans tout ce foisonnement, croyez-moi. C'est vraiment un sport difficile, rťservť aux spťcialistes. En temps qu'amateurs, vous n'aurez pas en principe ŗ faire l'analyse chimique dans un corps inconnu. Il sera bon cependant de pouvoir reconnaÓtre la prťsence des ťlťments chimique les plus courants dans les objets du ciel, comme l'hydrogŤne par exemple. Votre travail consiste plutŰt ŗ ťtudier une poignťes de raies seulement, dont on sait ŗ l'avance quels sont les ťlťments chimiques qui les produisent et qu'elles sont leurs longueurs d'ondes.
Alain - Je comprends bien ŗ prťsent le processus de production des raies, mais le spectre continu avec toutes ces nuances de couleurs, je ne vois pas d'oý il vient !
Aude - Un spectre de raies n'est possible que si les atomes baignent dans un gaz trŤs diluť. C'est une condition que l'on rencontre par exemple dans la chromosphŤre ou la couronne d'une ťtoile. Si la densitť de la matiŤre augmente et mÍme ŗ la limite, lorsque l'objet devient un solide, c'est l'agitation thermique des atomes qui est la cause des transitions atomiques. On montre que dans ce cas le corps ťmet une gamme continue d'ťnergie. Suivant que le corps est chaud ou froid le spectre d'ťnergie ťmis favorisera plutŰt les rayons bleus ou rouges respectivement. C'est l'origine de la couleur des ťtoiles.
Alain - Il suffit q'un corps soit chaud pour qu'il ťmette de la lumiŤre ?
Aude - Oui, et ceci est bien sur valable pour des solides. Par exemple, ne soyez pas ťtonnť que je vous dise que vos corps ťmettent de la lumiŤre. Mais cette lumiŤre n'est pas visible, car elle correspond au domaine spectral infrarouge. Si mes yeux ťtaient sensibles dans l'infrarouge, je vous verrai par l'ťmission continue infrarouge que vous produisez ŗ tout moment, mÍme par nuit noire !
Pour Ítre complet, je dirais qu'un autre mťcanisme, liť aux vibrations des molťcules, est susceptible de produire un spectre de raies. Dans le cas des ťtoiles, les molťcules n'existent que si la tempťrature est relativement basse, en dessous de 3000 K en gros. Lorsque la tempťrature est plus haute la structure des molťcules, qui est une association d'atomes, est brisťe. On trouve aussi la prťsence du spectre des molťcules dans les atmosphŤres planťtaires, le gaz mťthane par exemple dans le cas de Jupiter. Les raies molťculaires apparaissent trŤs nombreuses et accolťs les unes aux autres par paquets que l'on nomme des bandes.
Raymond - On voit comment les spectres prennent naissance. Mais tout ŗ l'heure Christian t'a posť une question sur la notion de rťsolution spectrale et de luminositť d'un spectrographe. Je suppose que se sont des caractťristiques de l'instrument qui permettent de mieux voir le spectre. Est-ce que tu peux prťciser ?
Aude - Une caractťristique importante du spectrographe sera sa capacitť ŗ sťparer des raies proches les unes des autres, afin par exemple de mieux distinguer l'empreinte des divers ťlťments chimiques qui constitue l'objet observť. On appelle pouvoir sťparateur spectral la plus petite distance entre deux raies qui permet de distinguer la duplicitť. Par exemple, un pouvoir sťparateur de 1 angstroms permettra de dťtecter la prťsence de deux raies distante de 1 angstroms dans le spectre. Si la distance entre ces deux raies est plus petite, l'observateur n'en verra qu'une seule, les deux composantes ťtant confondues. On dit que les raies ne sont sťparťes. Il y a donc une sorte de brouillage de l'information dans ce cas.
Raymond - Le meilleur spectrographe sera donc celui qui permettra de mieux sťparer les raies. C'est comme avec un tťlescope de qualitť qui permettra de voir de fins dťtails sur le disque de la planŤte Jupiter.
Aude - Au premier abord, on a tout intťrÍt en effet ŗ viser un pouvoir sťparateur permettant d'ťcarter au maximum les raies. Je rebondie cependant sur ton analogie avec l'observation visuelle de Jupiter. Pour bien rťsoudre les dťtails tu va devoir travailler avec un fort grossissement. Mais si tu conserve ce mÍme grossissement pour observer une faible galaxie tu risque de ne rien voir du tout. En effet, le grossissement de l'instrument est tel que tu va diluer dans le champ de l'oculaire la p‚le lumiŤre de la galaxie. De maniŤre naturelle tu va Ítre obligť d'adopter un grossissement bien plus faible. Cela se fera au dťtriment de la finesse des dťtails perÁus, mais au moins la galaxie deviendra visible, ce qui est bien l'essentiel. Nous avons le mÍme problŤme en spectrographie : soit choisir une trŤs bonne rťsolution spectrale, ce qui nous limite ŗ l'ťtude d'objets brillants, soit choisir une basse rťsolution spectrale et privilťgier la luminositť, ce qui permettra de saisir le spectre d'objets faibles.
Alain - En fait, on retrouve donc la notion de grossissement dans un spectrographe...
Aude - Oui, sauf qu'il s'agit ici d'une sorte de grossissement spectral. Il y a malheureusement un problŤme technique : il n'est pas facile de changer "l'oculaire" d'un spectrographe. Gťnťralement ce sera un instrument assez spťcialisť pour ťtudier tel type d'objet avec telle rťsolution. Le spectrographe universel qui permet de tout faire n'existe pas.
Alain - Je retrouve cela avec les tťlescopes. Suivant leurs conceptions, ils sont plus ou moins aptes ŗ faire de la haute rťsolution ou des objets faibles.
Aude - Exact.
Raymond - Cela signifie qu'il faut se spťcialiser ?
Aude - Oui, compte tenu de l'optimisation nťcessaire de l'instrument en fonction de la brillance des objets ťtudiťs ; mais aussi parce que le sujet est extrÍmement vaste et que votre carriŤre d'astronome n'y suffira pas ! Mais rien ne vous empÍche de construire plusieurs spectrographes si vous le souhaitez...
Alain - Qu'est-ce que tu nous conseille alors comme spectrographe, et pour quel type d'observations ?
Aude - Je vous propose un spectrographe ayant un pouvoir de rťsolution relativement modeste, pouvant sťparer des raies distantes de 10 angstroms environ. L'intťrÍt est que vous pourrez monter ce spectrographe directement au foyer d'un tťlescope relativement modeste, disons de la classe d'un LX200 de 8 pouces, comme le tiens Christian. Il sera suffisamment lumineux pour pouvoir enregistrer des spectres interprťtables d'ťtoiles de magnitude 13 au moins, toujours avec un tťlescope de 200 mm. Cela donne accŤs ŗ bon nombre d'ťtoiles ! Vous avez alors la puissance suffisante pour ťtudier le spectre d'un trŤs grand nombre d'ťtoiles variables, des novae, des comŤtes brillantes. Vous pourrez aussi prendre le spectre de nťbuleuses diffuses et planťtaires. En revanche, la plupart des supernovae se dťroberont... ŗ moins d'utiliser un tťlescope de la classe d'un 500 ou 600 mm. De la mÍme maniŤre, la rťsolution spectrale sera insuffisante pour ťtudier finement le mouvement des gaz autour d'astres possťdant des disques, comme la catťgorie des ťtoiles Be. Cependant, pour ce dernier type d'objet, vous serez en mesure de fournir des mesures spectrophotomťtriques de premiŤre importance.
Christian - Ca te parait les meilleures options pour dťbuter en spectroscopie ?
Aude - C'est bien sur un peu subjectif car ŗ chacun ces goŻts. La classe de performance que je viens de dťcrire est je pense un bon compromis entre le prix du spectrographe et la facilitť d'utilisation d'une part, et l'ťtendu des observations rťalisables d'autre part. Le maÓtre mot du dimensionnement que je vous propose est la compacitť et le poids le plus faible possible. De toute maniŤre, je vais essayer de vous donner le schťma de base d'un spectrographe, et il sera facile ŗ partir de lŗ de calculer l'instrument qui vous parait le plus opportun.
Retour ŗ la page d'accueil du stage Page prťcťdente Page suivante